Luciana Lorenzon, Dott.ssa in Psicologia, Psicoterapeuta, Psicofisiologa, Vice Presidente Biofeedback Federation of Europe (BFE), Certificata BCN e QEEG-D, Responsabile del Centro Italiano di Biofeedback e Neurofeedback
(membro CEI CT 324)
Introduzione – Quando l’ingegneria incontra il cervello
Negli ultimi anni, stiamo assistendo a una convergenza sempre più stretta tra ingegneria, intelligenza artificiale (AI) e neuroscienze. Al centro di questa evoluzione c’è la medicina di precisione, un approccio che si basa sulla raccolta e l’analisi di un’ampia quantità di dati biologici, clinici e ambientali, con l’obiettivo di arrivare, in un secondo momento, a personalizzare diagnosi e trattamenti in base al profilo unico di ogni paziente.
Questa visione, lanciata ufficialmente con il Precision Medicine Initiative negli Stati Uniti nel 2015, si fonda sull’integrazione di dati genetici, neurofisiologici e comportamentali per sviluppare terapie mirate, migliorare gli esiti clinici e ridurre l’approccio “standard” al trattamento. Nel campo della salute mentale, questo paradigma si traduce in ciò che oggi chiamiamo psichiatria di precisione: un modello che utilizza tecnologie avanzate per decifrare la complessità dei disturbi mentali, tenendo conto di fattori genetici, neurobiologici e ambientali.
Tuttavia, la natura eterogenea di questi disturbi rende difficile ottenere diagnosi precise basate solo su criteri sintomatici. È qui che entrano in gioco le neuroscienze computazionali e strumenti come il qEEG (quantitative electroencephalography), che permette di analizzare in dettaglio l’attività elettrica cerebrale. Combinando queste misurazioni con algoritmi di machine learning, si aprono nuove possibilità per individuare biomarcatori elettrofisiologici specifici, personalizzare le terapie e monitorare in modo oggettivo i risultati. Nel nuovo paradigma della salute mentale, il cervello viene letto come un sistema complesso ma misurabile, e l’ingegneria applicata ai segnali cerebrali diventa una chiave fondamentale per l’innovazione clinica.
Il qEEG e la psicofisiologia: misurare il cervello e leggere la mente attraverso i segnali
Tradizionalmente, l’elettroencefalografia (EEG) è stata utilizzata per rilevare l’attività elettrica cerebrale attraverso la registrazione dei segnali ottenuti da elettrodi posizionati sullo scalpo. Tuttavia, l’interpretazione dell’EEG convenzionale si è sempre basata sull’osservazione clinica e sull’esperienza dell’operatore, rendendo l’analisi spesso soggettiva.
Con il qEEG, questo approccio cambia radicalmente: il segnale EEG viene digitalizzato, elaborato con algoritmi matematici avanzati e confrontato con database normativi, consentendo un’analisi oggettiva, quantitativa e ripetibile dell’attività cerebrale. Il qEEG permette non solo di osservare quali frequenze cerebrali sono più o meno attive (come le onde delta, theta, alpha, beta e gamma), ma anche di capire come comunicano tra loro le diverse aree del cervello, attraverso l’analisi della connettività funzionale. Inoltre, consente di studiare la complessità del segnale e il modo in cui le reti cerebrali si organizzano e interagiscono tra loro.

Figura 1. Acquisizione di segnali cerebrali mediante EEG. Il soggetto indossa una cuffia EEG multicanale per la registrazione dell’attività elettrica cerebrale, visualizzata in tempo reale sul monitor. Questo tipo di configurazione viene utilizzato nelle valutazioni qEEG per analisi cliniche e ricerca neuroscientifica.
Grazie a strumenti avanzati come sLORETA, è possibile ottenere una mappatura tridimensionale dell’attività cerebrale, che aiuta a localizzare in modo più preciso le aree da cui proviene un’attività anomala o disfunzionale.
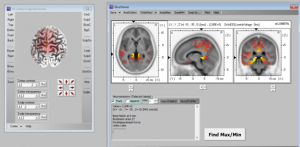
Figura 2. Ricostruzione dell’attività cerebrale con sLORETA. Visualizzazione tridimensionale delle aree cerebrali attive ottenuta dall’elaborazione dei segnali EEG. Le immagini mostrano come il software sLORETA consenta di localizzare in profondità l’attività elettrica del cervello, evidenziando le regioni coinvolte in specifici stati cognitivi o emotivi.
Questi strumenti permettono di osservare in tempo reale marker elettrofisiologici associati a disturbi psicopatologici come la depressione, l’ADHD o disturbi d’ansia, ma anche di valutare la risposta a trattamenti farmacologici o neuromodulativi, come la TMS (stimolazione magnetica transcranica).
Un aspetto fondamentale del qEEG in ambito clinico è il concetto di “fenotipo EEG”, ovvero insiemi di pattern ricorrenti nell’attività elettrica cerebrale che si osservano nella popolazione generale e che possono riflettere predisposizioni genetiche. Questi profili possono comparire in persone con diagnosi diverse, il che suggerisce che i sintomi psicologici o comportamentali non sempre corrispondono a un’unica configurazione cerebrale, ma piuttosto a una combinazione di tratti neurofisiologici che si intrecciano in modo complesso.
Questo modo di guardare al cervello consente di andare oltre le categorie diagnostiche tradizionali, come quelle dei manuali psichiatrici, e offre una prospettiva più biologica e personalizzata per comprendere la sofferenza mentale e scegliere i trattamenti più adatti. Per esempio, un’attività beta particolarmente elevata può essere associata a stati di iperattivazione, ansia o insonnia; una predominanza di onde theta nella regione frontale può riflettere difficoltà di attenzione e concentrazione, come accade spesso nei soggetti con ADHD; mentre un’eccessiva presenza di onde alfa nelle zone centrali del cervello è stata collegata a sintomi depressivi o a un certo distacco emotivo. A questi dati si aggiungono quelli che emergono dai potenziali evocati (ERP), che sono le risposte del cervello a stimoli sensoriali o cognitivi. Alcuni, come il P300 o il P50, aiutano a valutare aspetti fondamentali come la capacità di attenzione, la memoria operativa o il controllo degli impulsi, offrendo informazioni preziose sul funzionamento cognitivo individuale.
In sintesi, il qEEG rappresenta oggi uno degli strumenti più promettenti per portare oggettività e personalizzazione nella diagnosi e nella cura dei disturbi mentali. Un approccio che, integrando neuroscienze, psicofisiologia e tecnologia, si colloca perfettamente all’interno della medicina di precisione applicata alla salute mentale.
Oltre le diagnosi: nuovi cluster e cambio di paradigma
La psichiatria si confronta oggi con i limiti di un modello diagnostico basato su etichette sintomatiche come “depressione” o “ansia”, che raramente riflettono la reale complessità neurobiologica dei disturbi mentali. Diverse alterazioni cerebrali possono produrre sintomi simili, così come profili clinici differenti possono condividere lo stesso pattern cerebrale.
Da qui nasce l’esigenza di un nuovo approccio, basato su dati oggettivi e marcatori funzionali, più che su classificazioni rigide. Strumenti come il qEEG e i potenziali evocati (ERP) permettono di osservare in tempo reale l’attività cerebrale e di mappare le reti neurali coinvolte nei processi cognitivi ed emotivi. Il vero salto avviene quando questi dati vengono integrati con quelli genetici, ambientali e psicometrici, analizzati nel dettaglio con algoritmi di machine learning.
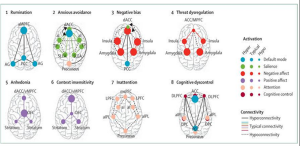
Figura 3. Pattern di connettività cerebrale alterata associati a diversi profili psicopatologici. Le mappe mostrano regioni chiave coinvolte e le variazioni nella connettività (iper-, ipo-, tipica), suddivise per domini sintomatologici (es. ruminazione, anedonia, discontrollo cognitivo).
Questo consente di individuare nuovi cluster clinici, fondati su pattern cerebrali condivisi piuttosto che su etichette diagnostiche. È questa la direzione della psichiatria computazionale, che non solo descrive la sofferenza mentale, ma aiuta a curarla in modo più mirato e personalizzato. Per riuscirci, serve una vera alleanza tra neuroscienze, ingegneria e scienza dei dati.
Ingegneria e algoritmi: il cuore tecnico del qEEG
Alla base della rivoluzione del qEEG c’è l’ingegneria: l’elaborazione digitale dei segnali (DSP), i modelli matematici e l’ottimizzazione dei dispositivi. Il segnale EEG grezzo è estremamente ricco di informazioni, ma anche vulnerabile a rumore, artefatti fisiologici (es. movimenti oculari, tensioni muscolari) e interferenze ambientali. L’ingegneria fornisce gli strumenti per trasformare questi segnali complessi in dati utili e interpretabili.
Uno degli approcci più usati è l’Independent Component Analysis (ICA), che permette di separare le fonti neurali da quelle non neurali, isolando attività cerebrali significative.
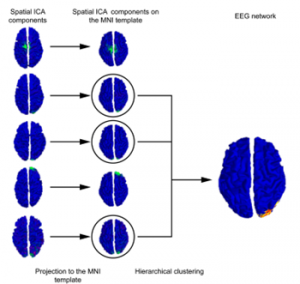
Figura 4. Ricostruzione di reti cerebrali EEG tramite ICA e clustering gerarchico. I componenti spaziali dell’EEG vengono proiettati su un template standard (MNI), raggruppati tramite clustering gerarchico e integrati in una rete cerebrale condivisa. Questo approccio consente di identificare pattern funzionali comuni tra soggetti a partire da segnali EEG.
Successivamente, l’attività viene mappata su aree funzionali corticali (es. Brodmann areas) e confrontata con database normativi basati su migliaia di soggetti sani.
Questa fase di comparazione statistica è fondamentale: consente di rilevare scostamenti significativi dal funzionamento cerebrale tipico, evidenziando iper- o ipo-attivazioni, anomalie di connettività o pattern atipici di sincronizzazione.
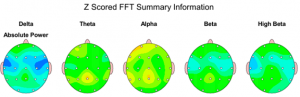
Figura 5. Mappe EEG Z-score basate su database normative. Distribuzione della potenza assoluta nelle principali bande di frequenza (Delta, Theta, Alpha, Beta, High Beta), calcolata tramite FFT e normalizzata rispetto a un database normativo.
I software moderni integrano anche metodi avanzati di visualizzazione tridimensionale (come sLORETA) che permettono di localizzare in profondità le fonti dell’attività cerebrale, con una precisione sempre maggiore.
In parallelo, l’uso di strumenti di de-artifacting automatizzato aumenta la qualità dei dati, rendendo il qEEG sempre più affidabile anche in ambienti clinici meno controllati.
In questo scenario, l’ingegnere diventa una figura chiave nella progettazione di pipeline di analisi, nella validazione dei dati, nella costruzione di sistemi embedded per dispositivi portatili e nella traduzione delle metriche cerebrali in interfacce comprensibili e utilizzabili dai clinici.
AI e machine learning nella lettura dei dati cerebrali
Se l’ingegneria consente di ripulire e organizzare i segnali cerebrali, è l’intelligenza artificiale a fare il passo successivo: permette di scoprire ciò che non si vede a occhio nudo, come schemi nascosti nei dati, relazioni complesse e sottotipi clinici che sfuggono alle classificazioni tradizionali.
Nel contesto del qEEG, gli algoritmi di machine learning supervisionato vengono utilizzati per distinguere tra condizioni già note (ad esempio, tra un paziente depresso e un soggetto sano). Ma è con i modelli non supervisionati che si apre la strada alla scoperta: l’intelligenza artificiale può individuare nuovi cluster di funzionamento cerebrale, come diversi sottotipi di (Post-Traumatic Stress Disorder) o forme di depressione resistente, che richiedono trattamenti differenti.
Tecniche come reti neurali, support vector machines (SVM), sparse clustering o modelli ad albero decisionale vengono oggi applicate su ampi database EEG raccolti in più centri di ricerca. I risultati sono promettenti: è possibile identificare biotipi cerebrali associati a una diversa risposta ai trattamenti, migliorare la previsione dell’efficacia terapeutica e persino definire protocolli di neuromodulazione personalizzata.
Un esempio concreto è l’uso della Power Envelope Connectivity (PEC), una tecnica che consente di misurare la connettività cerebrale in modo più accurato, superando il problema delle interferenze tra segnali. In uno studio multicentrico, i dati ottenuti con il qEEG sono stati confrontati con immagini da risonanza magnetica funzionale (fMRI), e i due metodi hanno identificato in modo coerente gli stessi sottotipi clinici. Un risultato potente, che dimostra come neurotecnologia e intelligenza artificiale, insieme, possano portare la psichiatria a un nuovo livello di precisione.
L’obiettivo non è sostituire il clinico, ma amplificarne la capacità di lettura: non più solo osservatore di sintomi, ma interprete dei circuiti cerebrali che li generano.
Neurofeedback e interfacce cervello-macchina: applicazioni cliniche
Uno degli sviluppi più concreti dell’integrazione tra qEEG e AI è il neurofeedback personalizzato, un trattamento non invasivo che utilizza i dati EEG del paziente per guidare sessioni di autoregolazione cerebrale.
Il processo inizia con un assessment qEEG e la definizione di un profilo funzionale individuale. Attraverso sessioni strutturate, il paziente riceve feedback audiovisivo in tempo reale legato alla propria attività cerebrale. L’obiettivo è favorire la neuroplasticità e la stabilizzazione di pattern cerebrali più funzionali.
In parallelo, la tecnologia EEG viene impiegata nello sviluppo di interfacce cervello-macchina (BCI), che consentono a soggetti con disabilità motorie di controllare dispositivi esterni tramite il pensiero. Elettrodi a secco, algoritmi embedded, e sistemi a bassa latenza rendono queste interfacce sempre più reattive e indossabili.
Le applicazioni cliniche spaziano dalla riabilitazione cognitiva post-ictus, al trattamento di disturbi dell’attenzione, fino alla domotica controllata dal pensiero in soggetti con gravi paralisi. Il qEEG qui non è solo strumento diagnostico, ma tecnologia abilitante, che connette il cervello al mondo esterno.
Standardizzazione e dispositivi portatili: sfide e prospettive
Perché il qEEG diventi davvero uno strumento diffuso nella pratica clinica quotidiana, è necessario affrontare due grandi sfide: la standardizzazione e la portabilità.
Sul piano normativo, servono protocolli chiari per l’acquisizione, l’elaborazione e l’interpretazione dei dati EEG. Le discrepanze tra diversi database, la variabilità dei protocolli e la mancanza di validazione cross-sito rappresentano ostacoli ancora da superare. L’adozione di standard internazionali, come quelli promossi dal progetto High 5s della WHO o dalla normativa CE/FDA, è un passaggio cruciale.
Parallelamente, l’evoluzione tecnologica sta portando a dispositivi sempre più miniaturizzati, wireless e a basso impatto, dotati di elettrodi a secco, con acquisizione in cloud e integrazione con app mobile. Questi dispositivi consentono il monitoraggio continuo, anche al di fuori del contesto clinico, aprendo la strada alla neuro-prevenzione, al supporto al benessere mentale, e persino alla personalizzazione delle esperienze cognitive (es. apprendimento, performance sportiva, mindfulness).
Il futuro del qEEG sarà probabilmente ibrido: una combinazione tra strumenti ad alta precisione per la clinica e dispositivi portatili per il supporto quotidiano.
Conclusione: ripensare la salute mentale con ingegneria e neuroscienze
Il qEEG non è solo uno strumento tecnico. È un ponte tra ingegneria e medicina, tra dati e mente, tra tecnologia e cura. In un’epoca in cui la sofferenza mentale cresce e si diversifica, abbiamo bisogno di strumenti nuovi, capaci di cogliere l’unicità di ogni individuo.
Superare le diagnosi rigide, individuare marcatori biologici personalizzati, sviluppare trattamenti mirati: tutto questo è possibile solo se neuroscienze, ingegneria e intelligenza artificiale imparano a lavorare insieme.
Il futuro della psichiatria sarà computazionale, psicofisiologico e personalizzato. E chi progetta sistemi, scrive algoritmi o costruisce interfacce non sarà più solo un tecnico, ma un alleato della salute mentale.
















 Archivio Numeri
Archivio Numeri





